|
※サムネイル画像をクリックすると拡大画像が表示されます。
Norgen社Plasma/Serum RNA/DNA Purification Mini Kitの使用手順フローチャート。
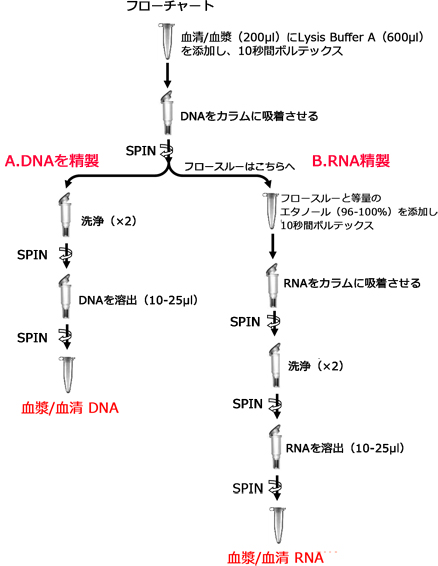
図1. 血漿サンプル量の違いによるRNA量の比較。EDTA処理した血漿サンプル(50μL, 100μL, 200μL)から血液循環RNAを精製した。精製RNAを鋳型にmiR-21(図1A)およびハウスキーピング遺伝子5s rRNA(図1B)をRT-PCRによって測定した。miR-21および5s rRNAの転写産物はサンプル量に応じて直線的に増加した。
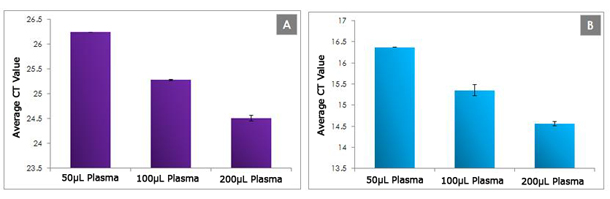
図2. 溶出バッファー量の違いによるRNA抽出効率の検討。EDTA処理した血漿サンプルを200μL用いて、異なる溶出容量(10μL,15μL,25μL)によってRNA抽出を行った。 精製RNAを鋳型にmiR-21(図2A)およびハウスキーピング遺伝子5s rRNA(図2B)についてRT-PCRによって測定した。 溶出バッファーの量を減らすことによって、いずれのRNAについても効率よく濃縮できた。

図3. 他社製品との比較。図3A.Norgen(NOG)社キットおよび各社RNA精製キットを用いて精製したRNAを鋳型にmiR-21についてRT-PCRを行った。NOG社キットは他社品と比較して高効率で分離・精製することがわかる。
図3B.NOG社キットおよび各社DNA精製キットを使用して精製したDNAを鋳型に5S rRNA 遺伝子について定量PCRを行った。NOG社キットは他社品と比較して高効率で分離・精製することがわかる。
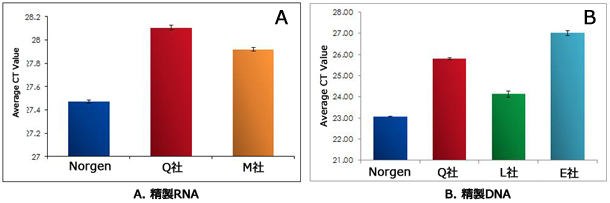
図4. PCR反応を阻害する夾雑物の影響。Norgen(NOG)社キットおよび各社DNA精製キットから抽出したDNAについて、異なる鋳型量(3μL, 6μL, 9μL)を用いて5S rRNA遺伝子を定量的PCRで測定した。鋳型量を増やした際のCt値の上昇は、PCR阻害を起こす夾雑物の増加が影響している。NOG社キットでは、鋳型量を増やした場合においても、PCR反応への影響は見られなかった。

Norgen社Plasma/Serum RNA/DNA Purification Mini Kit。
|

|
|
Norgen社Plasma/Serum RNA/DNA Purification Mini Kitの使用手順フローチャート。
|
|
|
| メーカー |
品番 |
包装 |
|
NOG
|
55200
|
50 PREP.
|
※表示価格について
| 当社在庫 |
なし
|
| 納期目安 |
1週間程度
|
| 法規制 |
安・化管
|
| 保存温度 |
常温
|
|
※当社では商品情報の適切な管理に努めておりますが、表示される法規制情報は最新でない可能性があります。
また法規制情報の表示が無いものは、必ずしも法規制に非該当であることを示すものではありません。
商品のお届け前に最新の製品法規制情報をお求めの際はこちらへお問い合わせください。
|
※当社取り扱いの試薬・機器製品および受託サービス・創薬支援サービス(納品物、解析データ等)は、研究用としてのみ販売しております。
人や動物の医療用・臨床診断用・食品用としては、使用しないように、十分ご注意ください。
法規制欄に体外診断用医薬品と記載のものは除きます。
|
|
※リンク先での文献等のダウンロードに際しましては、掲載元の規約遵守をお願いします。
|
|
※CAS Registry Numbers have not been verified by CAS and may be inaccurate.
|






